
Was ist die EUDAMED?
Die Europäische Datenbank für Medizinprodukte (EUDAMED) ist eine digitale Plattform und Datenbank, die von der Europäischen Kommission im Rahmen der Umsetzung der MDR (Medical Device Regulation) und der IVDR (In Vitro Diagnostic Regulation entwickelt wurde.
Sie dient als Informations-Datenbank über den gesamten Lebenszyklus von Medizinprodukten und IVDs, die in der EU bereitgestellt werden. Die verpflichtende Nutzung von EUDAMED beginnt nach offizieller Bekanntgabe der Funktionsfähigkeit der Module.
Welche EUDAMED-Module gibt es?
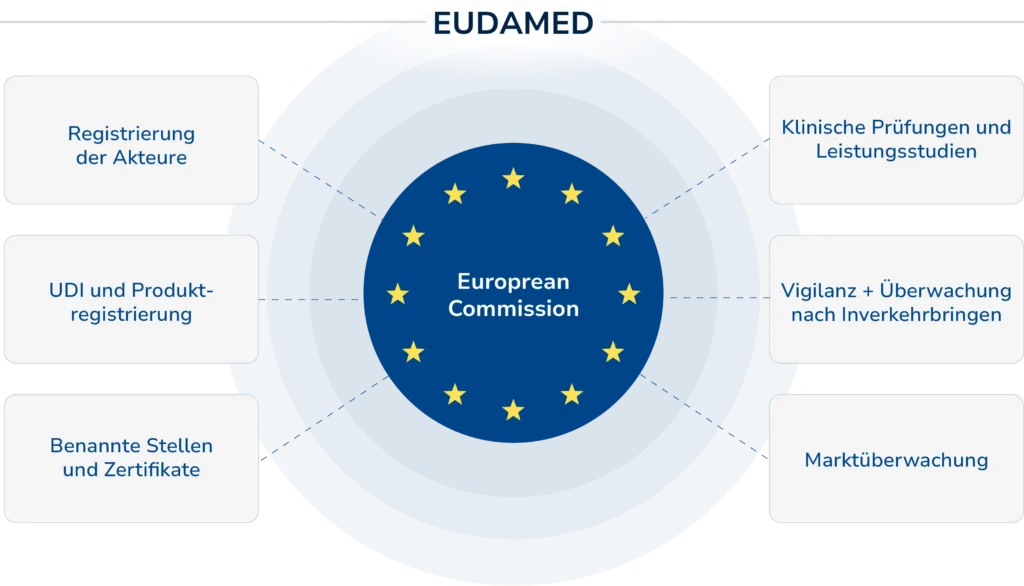
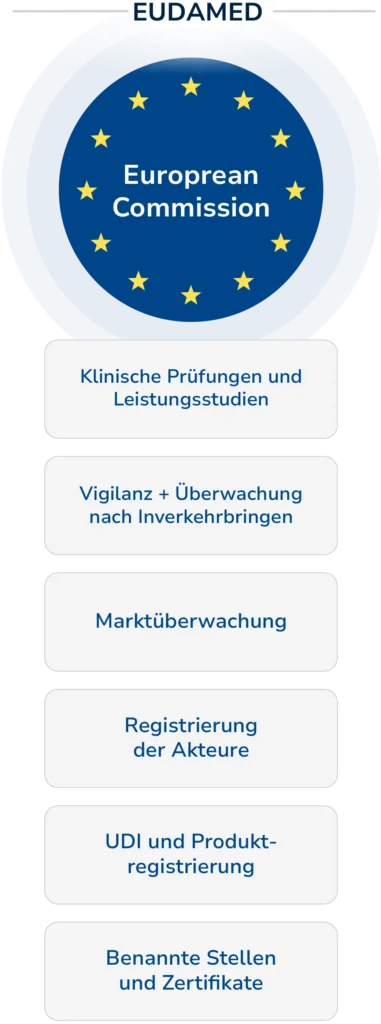
EUDAMED besteht aus einer öffentlichen Website und sechs Modulen:
- Registrierung der Akteure
- Eindeutige Produktidentifikation (Unique Device Identification, UDI) und Produktregistrierung
- Benannte Stellen und Zertifikate
- Klinische Prüfungen und Leistungsstudien
- Vigilanz und Überwachung nach Inverkehrbringen
- Marktüberwachung
Einige Module (z. B. Akteureregistrierung, UDI/Produkt und Benannte Stellen/Zertifikate) sind bereits verfügbar und können genutzt werden. Die restlichen Module werden schrittweise ausgerollt. Den aktuellen Zeitplan bis zur vollständigen Funktionsfähigkeit der EUDAMED stellt die Europäische Kommission zur Verfügung.
Welche EUDAMED-Module sind für Ihre Produkte oder Studien relevant? Wir begleiten gerne die Registrierung und Einbindung. Jetzt Kontakt aufnehmen!
– David Brodbeck, Abteilungsleiter Auftragslabor

Das könnte Sie auch interessieren

Diagnostik

Pharma

EUDAMED kurz erklärt
Abkürzungen
EU: Europäische Union
EUDAMED: Europäische Datenbank für Medizinprodukte
IVD: In-vitro-Diagnostika
IVDR: In Vitro Diagnostic Regulation
MDR: Medical Device Regulation
UDI: Unique Device Identification, Eindeutige Produktidentifikation

